- 服務(wù)
- ·
circRNA-seq
- 產(chǎn)品介紹
- 案例解析
- 結(jié)果展示
- 送樣建議
- FAQ
服務(wù)介紹
利用circRNA對(duì)RNase R的耐受性從而富集circRNA,去rRNA后進(jìn)行鏈特異建庫(kù),采用Illumina平臺(tái)對(duì)circRNA文庫(kù)進(jìn)行測(cè)序,通過生信分析得到circRNA的表達(dá)結(jié)果。
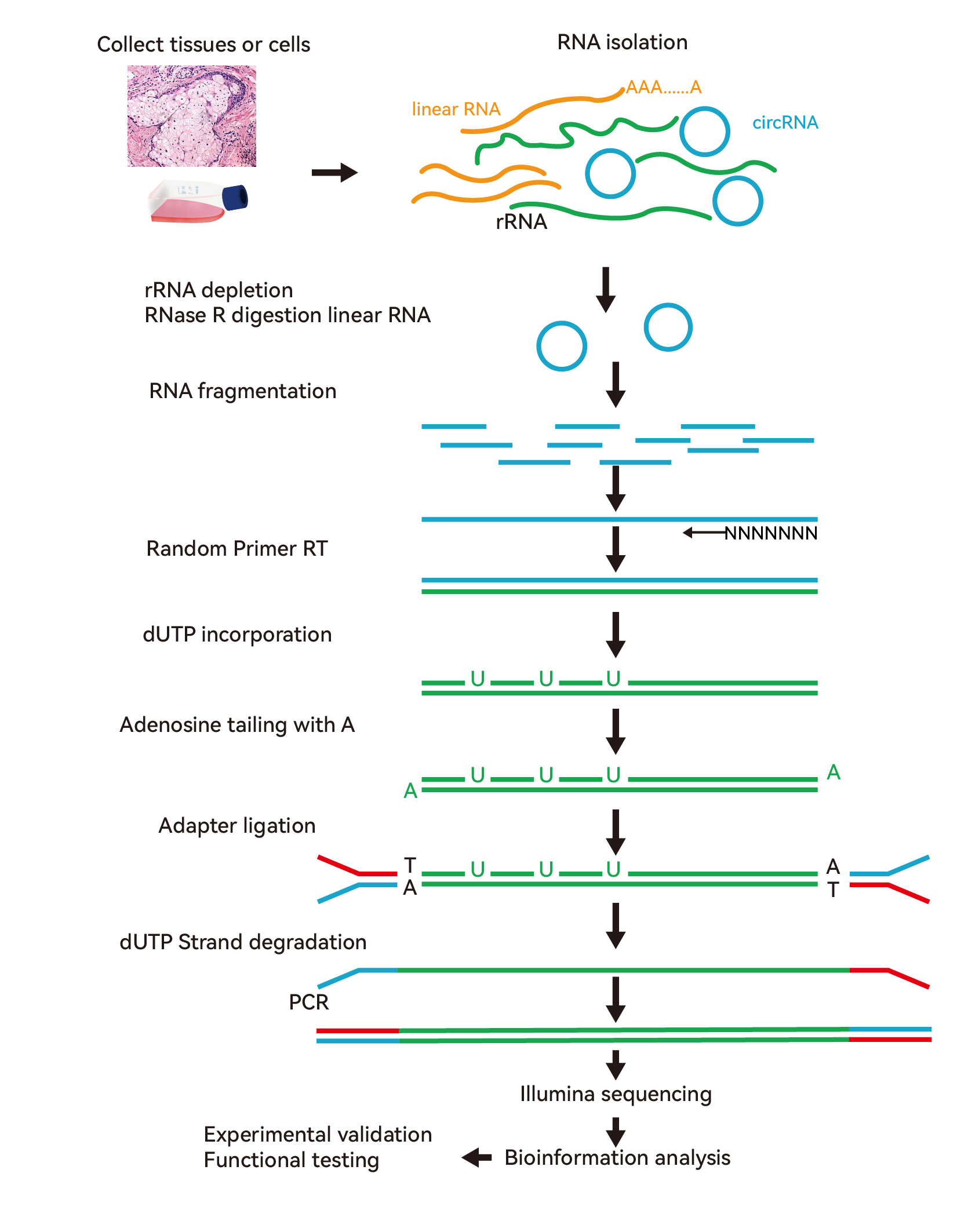
circRNA測(cè)序技術(shù)路線
測(cè)序方案
測(cè)序平臺(tái):Illumina Novaseq 6000/NovaSeq X Plus
測(cè)序模式:PE150
測(cè)序數(shù)據(jù)量:10 Gb raw data
人喉鱗狀細(xì)胞癌中circRNA的RNA-seq表達(dá)譜
RNA-Seq profiling of circular RNAs in human laryngeal squamous cell carcinomas
Lu et al. Molecular Cancer (2018) 17:86(IF:6.204)
測(cè)序策略:circRNA測(cè)序(RNase R+)
樣本分組:10例,5例腫瘤組織(2例高分化,3例中分化),5例正常組織
人喉鱗狀細(xì)胞癌(LSCC)是起源于喉黏膜上皮組織的惡性腫瘤,是頭頸部腫瘤中惡性程度非常強(qiáng)的腫瘤,世界范圍內(nèi)每年發(fā)生率占比2.4%,近年內(nèi)還有逐漸增加趨勢(shì)。本研究主要關(guān)注circRNA在LSCC疾病中的表達(dá)情況。研究者選擇10例LSCC患者臨床組織標(biāo)本(2例高分化、3例為中分化、 5例正常)進(jìn)行RNA高通量測(cè)序,分析樣本中circRNA表達(dá)情況。共鑒定出21444個(gè)circRNA,其中在LSCC樣本中顯著上調(diào)的circRNA 29個(gè),顯著下調(diào)circRNA 19個(gè),進(jìn)一步結(jié)合臨床特征(高分化,中分化和正常)進(jìn)行分類,將差異表達(dá)circRNA縮小到18個(gè)和5個(gè)(圖1)。CircRNA-miRNA-mRNA調(diào)控網(wǎng)絡(luò)預(yù)測(cè)分析,發(fā)現(xiàn)20個(gè)失調(diào)控circRNA與多種腫瘤相關(guān)的miRNA相關(guān),信號(hào)通路KEGG富集分析發(fā)現(xiàn),過氧化物酶體PPAR、軸突導(dǎo)向、Wnt和細(xì)胞周期通路與LSCC密切相關(guān)(圖2)。隨后的qPCR驗(yàn)證結(jié)果顯示(圖3),has_circ:chr20:31876585-31,897,648可以很好區(qū)分LSCC標(biāo)本和正常標(biāo)本,表明circRNA可作為L(zhǎng)SCC潛在的理想標(biāo)志物。
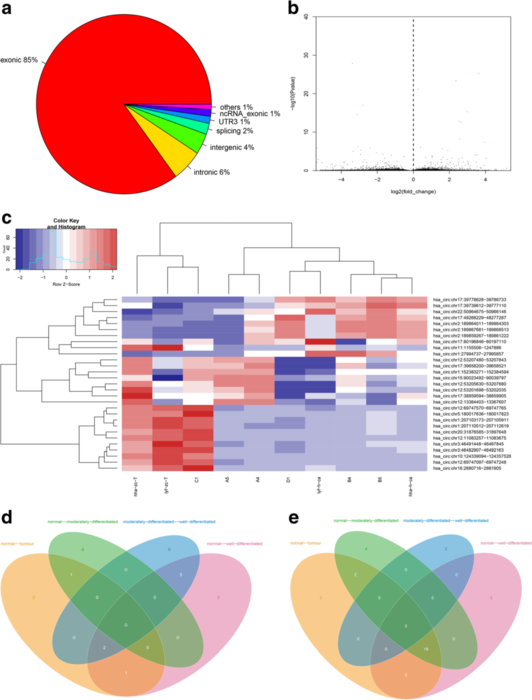
圖1 LSCC樣本中circRNA差異表達(dá)譜
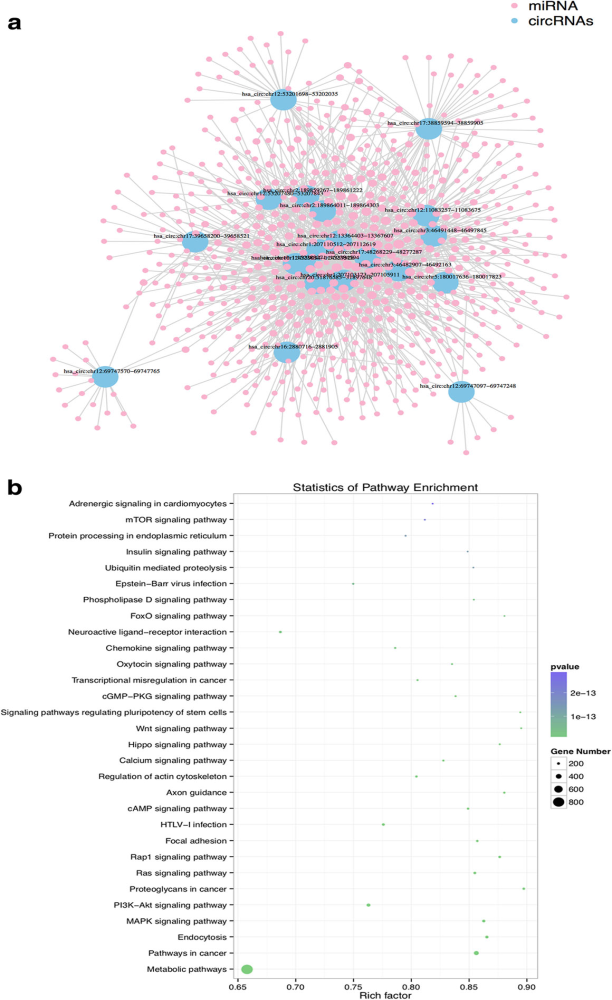
圖2 CircRNA及靶向miRNA網(wǎng)絡(luò)調(diào)控圖與KEGG代謝通路富集分析
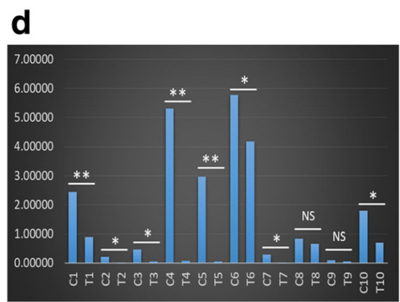
圖3 hsa_circ:chr20:31876585–31,897,648在10對(duì)LSCC腫瘤樣本及正常樣本中的Q-PCR驗(yàn)證
生物信息分析
基礎(chǔ)分析
原始數(shù)據(jù)質(zhì)控檢查
比對(duì)結(jié)果質(zhì)控檢查
基因覆蓋度分析
circRNA預(yù)測(cè)及鑒定
circRNA序列預(yù)測(cè)
基于circRNA表達(dá)的樣品主成分分析
高級(jí)分析
circRNA差異分析
差異circRNA宿主基因的GO功能分析
差異circRNA宿主基因的KEGG通路分析
差異circRNA宿主基因的Rectome通路分析
差異circRNA的靶向miRNA預(yù)測(cè)分析
差異circRNA及靶向miRNA網(wǎng)絡(luò)調(diào)控制圖
部分結(jié)果示例
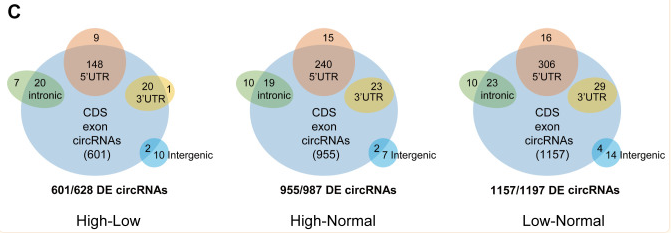
圖1. 根據(jù)不同的基因組位點(diǎn)(外顯子、內(nèi)含子、反義、基因內(nèi)和基因間)對(duì)表達(dá)差異顯著的circRNA進(jìn)行分類
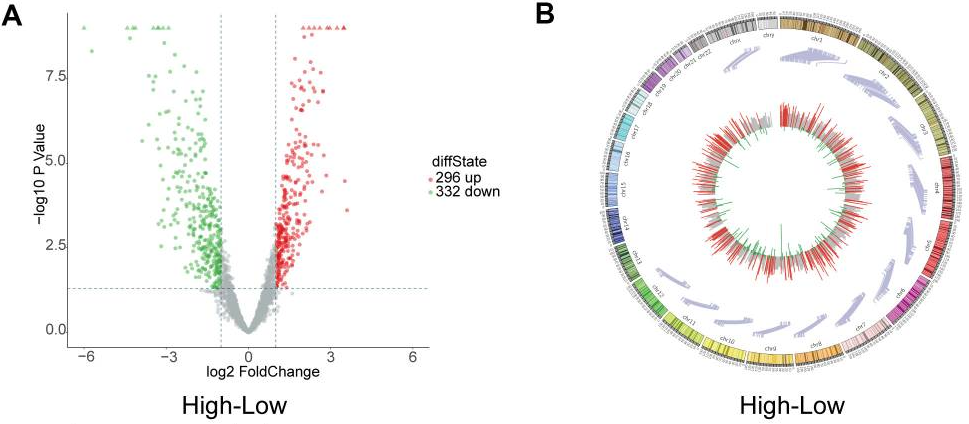
圖2. 繪制火山圖、Circos圖揭示每個(gè)circRNA在人類染色體上的位置
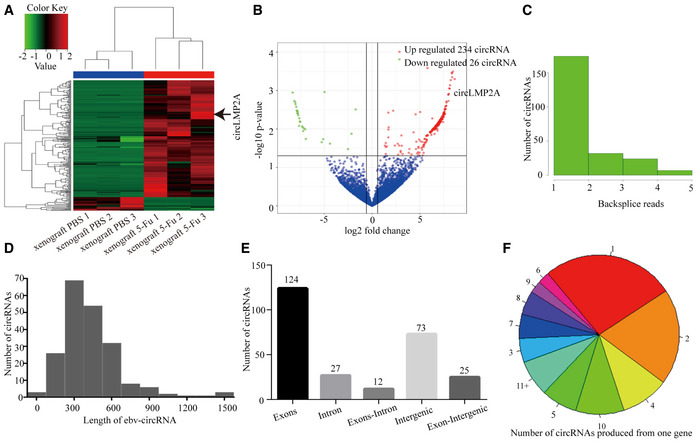
圖3. 熱圖、火山圖分析circRNA的表達(dá)差異倍數(shù)
Table.circRNA-seq原始樣本送樣建議
送樣類型
送樣量
備注
細(xì)胞 (細(xì)胞數(shù))
≥1*10^6
無(wú)支原體污染
動(dòng)物組織
≥100mg
植物組織
≥100mg
全血
≥4mL
FFPE
8-10片,未染色,厚度10μm
Table.circRNA-seq RNA樣本送樣建議
送樣類型
送樣量
完整性(RIN值)
濃度
其他
純度
total RNA(組織、細(xì)胞、全血等)
≥4ug
≥7
≥100ng/μl
無(wú)DNA,蛋白/鹽離子等污染,樣本無(wú)色透明不粘稠
FFPE組織RNA
≥4ug
≥3
/
DV200>30%
*更具體的送樣方法請(qǐng)咨詢銷售或技術(shù)支持
物種范圍:人、小鼠、大鼠等哺乳動(dòng)物,擬南芥、水稻、番茄、玉米、大豆等植物,其他物種詳詢銷售或技術(shù)支持
Q1:circRNA測(cè)序與全轉(zhuǎn)錄組測(cè)序有什么不同?
A1:全轉(zhuǎn)錄組測(cè)序采用去rRNA鏈特異性的建庫(kù)方式,數(shù)據(jù)分析內(nèi)容包含了mRNA、lncRNA及circRNA全部信息,數(shù)據(jù)質(zhì)量較好。CircRNA測(cè)序采用去rRNA去線性鏈特異性的建庫(kù)方式,通過RNase R 消化線性RNA從而富集circRNA,對(duì)建庫(kù)起始量要求較高(一般大于2μg),測(cè)序數(shù)據(jù)質(zhì)量較全轉(zhuǎn)錄組稍差,但可將circular junction reads數(shù)提高10倍以上,更適合專注circRNA研究的項(xiàng)目。
填寫需求描述給我們
工具快速咨詢
400-8989-400
geneseed@geneseed.com.cn

 購(gòu)物車
購(gòu)物車




 廣州市黃埔區(qū)開源大道11號(hào)科技企業(yè)加速器A區(qū)6棟2樓
廣州市黃埔區(qū)開源大道11號(hào)科技企業(yè)加速器A區(qū)6棟2樓


 geneseed@geneseed.com.cn
geneseed@geneseed.com.cn