- GENESEED

- 首頁
- >
- GENESEED
- >
Nat Commun | 余佳益團隊利用cis核酶合成的circRNA表達Cas13有效對抗RNA病毒
撰文:EP編輯:circRNA
排版:Siuyee
研究背景
通過遞送編碼蛋白質的RNA,實現異位蛋白質功能是一種新的治療策略。而環狀RNA(circRNA)是一種最先進的延長RNA功能的策略。circRNA體外制備可以利用化學或酶連接方法,以及目前流行的利用I族內含子的RNA自剪接的circRNA形成策略。
基于RNA剪接的環化策略可以在體外和體內產生大量circRNA,但由于剪接需消耗一定RNA序列長度。盡管GTP和Mg2+在體外加速PIE剪接,但剪接后的小副產物RNA仍需要額外的去除步驟。
2024年8月4日,中國臺灣國家衛生研究院余佳益研究團隊在Nature Communications雜志在線發表研究論文:A cis-acting ligase ribozyme generates circular RNA in vitro for ectopic protein functioning。該研究利用系統篩選順式連接酶核酶(RzL)體外合成circRNA,并針對合成的circRNA進行一系列驗證表明,一個內部核糖體進入位點(IRES)使circRNA能夠翻譯,但兩個順式的IRES阻礙了翻譯。加上特異的引導RNA,表達核糖核酸酶Cas13的circRNA顯示出對抗相應RNA病毒的良好潛力,進一步拓寬了circRNA的應用。


一、PIE剪接策略合成RNase R抗性circRNA,可利用RT-PCR量化
首先,研究利用傳統PIE策略建立circRNA的生產、鑒定和量化平臺,但也留意到剪接反應中伴隨小片段RNA副產物產生。(圖1)
二、連接酶核酶(RzL)及其位于RNA 5 '和3 '端的底物,在體外自主催化RNA環化
接著,研究合成含有相同蛋白質翻譯框,但兩側有RzL和底物序列的poR2載體,進行體外轉錄,并以RzL匹配的相應底物RNA (SUB)加尾,使線性RNA前體可直接自連接形成circRNA。為驗證RzL介導RNA環化的有效性,研究添加polyA聚合酶,以便更好地可視化和評估高效的RNA環狀化。
結果表明,沒有添加RzL的RNA具有poly A,而添加RzL和SUB的大部分RNA不受影響。另一方面,研究利用RNase R處理,檢測circRNA環化效率約為75-100%;PIE介導的環化效率約為50%以上,在熱量和GTP增強的情況下達到75%以上。(圖1)
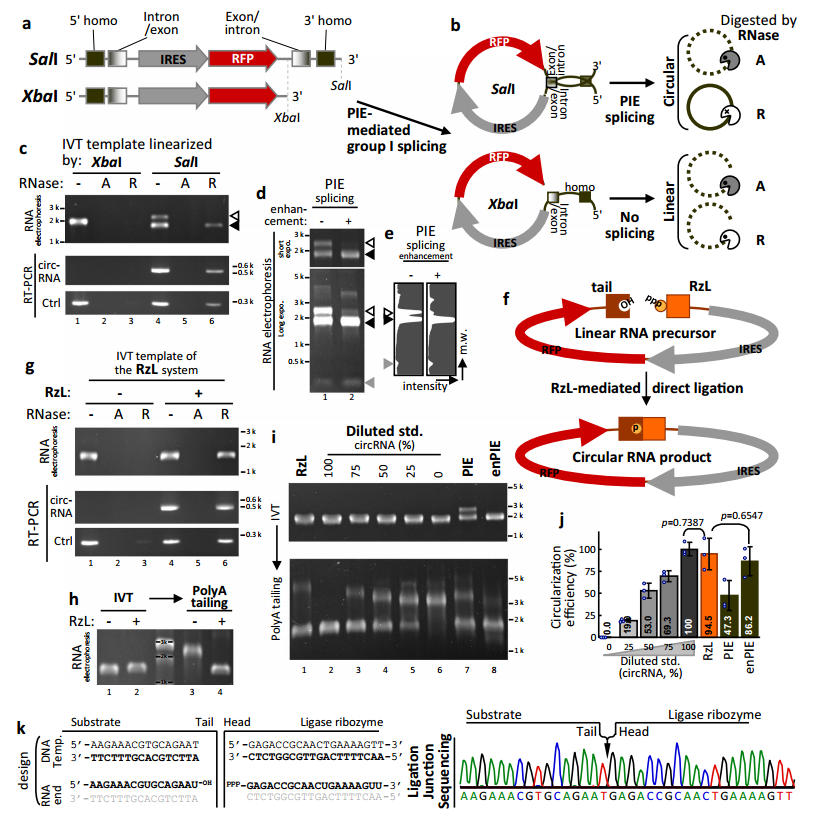
圖1 傳統內含子-外顯子(PIE)方法以及連接酶核酶(RzL)催化circRNA生成策略的建立。
三、RNA修飾影響RzL-SUB形成circRNA
研究表明低至1%的m6A或m5C修飾輕微影響circRNA的形成,用m6A替換所有的A完全阻斷circRNA的形成,用m5C替換所有的C只輕微阻礙circRNA的形成。然而,m5C修飾的circRNA仍然無法表達蛋白質,這可能是因為m5C阻礙了翻譯所需的IRES結構,或者是因為m5C介導的翻譯抑制。
此外,RzL催化核心的兩個核苷酸T和G替換為G和C的突變也幾乎抑制了RzL的RNA連接活性。平末端PCR產物作為IVT模板時,T7 RNA聚合酶在3 '末端添加了一個外部的非模板核苷酸,會干擾RNA的環化。(圖2)
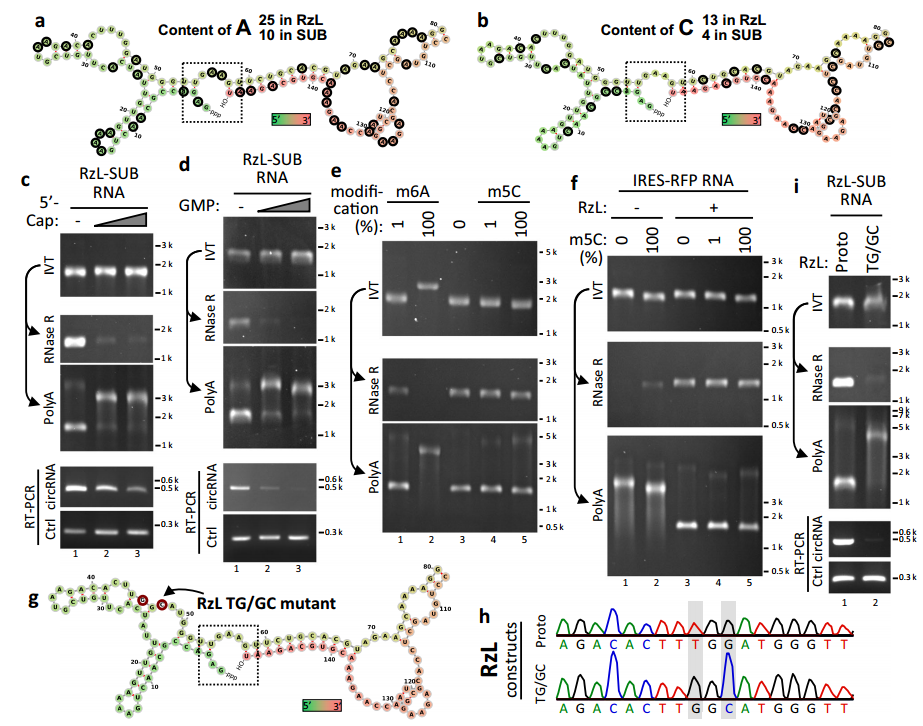
圖2 RNA修飾影響RzL催化circRNA形成。
四、具有兩個IRES的circRNA會阻礙彼此的蛋白表達
研究發現在一個circRNA表達Fluc和GFP融合蛋白,或利用2a介導的核糖體跳躍分割FLuc和GFP序列,或在一個circRNA中用兩個相同的IRES分別指導FLuc和GFP的翻譯,表達的熒光及FLuc活性都不如兩個circRNA分別表達的強,可能是外部IRES中的cis,而非trans阻礙了circRNA的翻譯(圖3)
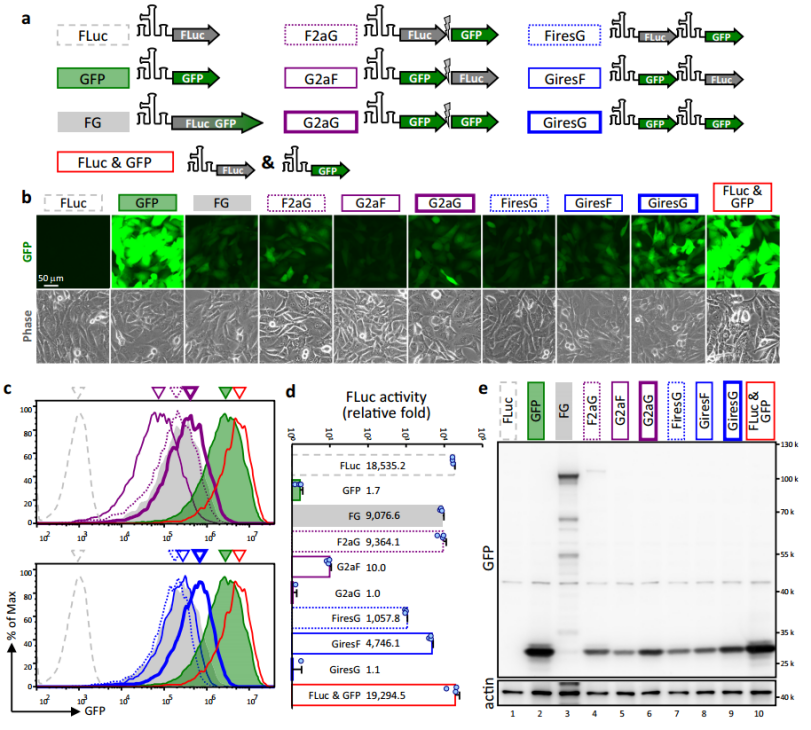
圖3 外部IRES中的cis,而非trans阻礙了circRNA的翻譯。
五、高翻譯效率可能賦予circRNA抗病毒潛能
研究團隊考慮到黃病毒(JEV)RNA可以復制并隱藏在ER相關膜結構中,通過circRNA表達修飾的Cas13以靶向ER (erCas13)。單獨遞送erCas13 circRNA顯示出基礎抗病毒活性,并利用GFP指示病毒的感染情況,未遞送RNA組的GFP(+)率達到~81%時,erCas13 circRNA將病毒感染抑制至GFP(+)率低約63%。添加sgRNA, erCas13 circRNA可以進一步將病毒感染降低至~45% GFP(+)。轉染erCas13線性mRNA或circRNA后,都持續表現出一定水平的抗病毒活性。然而,與mRNA相比,erCas13 circRNA翻譯更多的erCas13,以幫助sgRNA獲得更好的抗病毒活性。(圖4)
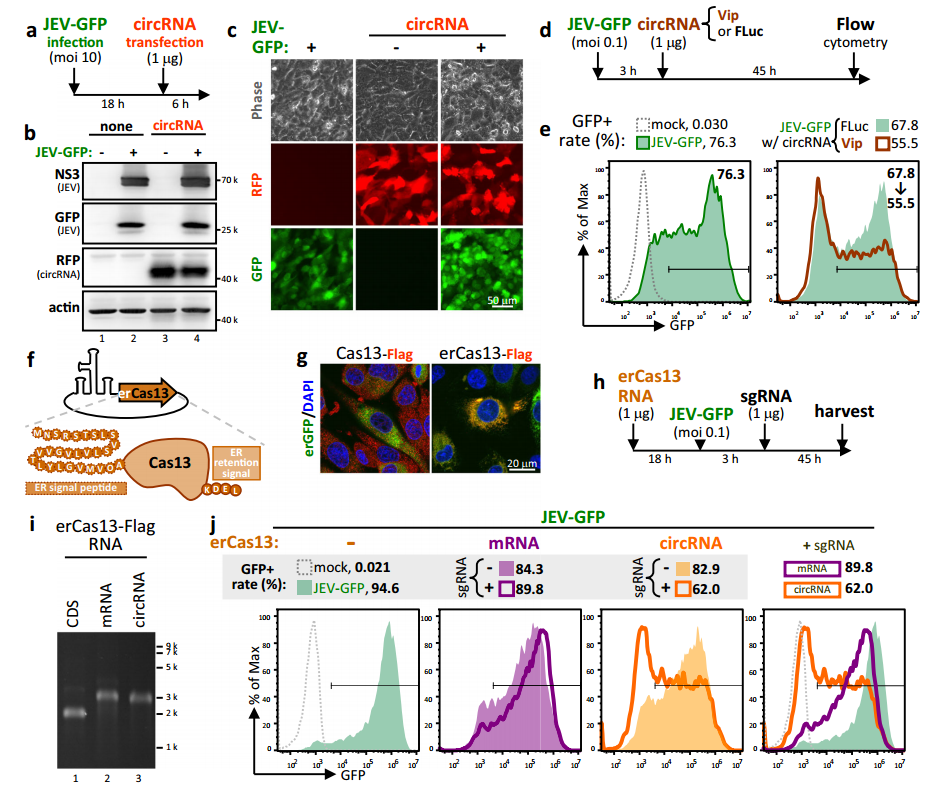
圖4 IRES驅動表達erCas13的circRNA可能對重組RNA病毒JEV-GFP具有抗病毒作用。
總結
研究通過系統篩選的順式作用連接酶核酶(RzL)對單鏈RNA進行共價環化,研究最小化了RzL作用所需的RNA序列。RzL策略在體外轉錄(IVT)過程中招募了一個攜帶5'-三磷酸基團 (ppp)的RzL,并直接和自主地加入到3 '端相應的底物序列中。與GTP促進circRNA形成的剪接方法不同,RzL策略高度依賴于酶-底物RNA配對產生circRNA而沒有副產物RNA。此外,團隊研究了表達兩種蛋白circRNA的翻譯特性,并驗證了編碼Cas13 circRNA的抗RNA病毒潛能,這為circRNA在外源蛋白功能和應用方面的研究提供了重要信息。
原文鏈接
https://www.nature.com/articles/s41467-024-51044-y?

 購物車
購物車


 廣州市黃埔區開源大道11號科技企業加速器A區6棟2樓
廣州市黃埔區開源大道11號科技企業加速器A區6棟2樓


 geneseed@geneseed.com.cn
geneseed@geneseed.com.cn